巴氏吸管由醫(yī)用級聚乙烯(PE)制成,管體
近期細(xì)胞自噬領(lǐng)域重要研究進(jìn)展一覽
本文中,,小編整理了近期細(xì)胞自噬領(lǐng)域的重要研究成果,分享給大家,!

【1】Nat Commun:自噬或是休眠乳腺癌細(xì)胞復(fù)發(fā)的罪魁禍?zhǔn)字?/p>
doi:10.1038/s41467-018-04070-6
腫瘤在初次診斷和治療后復(fù)發(fā)是導(dǎo)致乳腺癌病人死亡的主要原因,,因?yàn)樾菝叩哪[瘤細(xì)胞會轉(zhuǎn)移性爆發(fā)。腫瘤微環(huán)境的改變可以促使激活休眠細(xì)胞的信號通路從而導(dǎo)致它們增殖,。但是研究人員并不知道涉及轉(zhuǎn)移的休眠乳腺癌細(xì)胞短期及長期存活的過程,。
近日,來自美國國立衛(wèi)生院和德克薩斯大學(xué)MD安德森癌癥中心的科學(xué)家在癌癥研究所癌癥生物學(xué)和遺傳學(xué)部Kent W. Hunter和Jeffrey E. Green教授的帶領(lǐng)下發(fā)現(xiàn)自噬是轉(zhuǎn)移性休眠乳腺癌細(xì)胞生存的一種關(guān)鍵機(jī)制,。使用藥物或者遺傳學(xué)手段抑制休眠乳腺癌細(xì)胞的自噬可以顯著抑制小鼠以及人類乳腺癌臨床前休眠3D模型中癌細(xì)胞的存活時(shí)間以及轉(zhuǎn)移灶的形成,。
通過體內(nèi)實(shí)驗(yàn),研究人員發(fā)現(xiàn)自噬基因自噬相關(guān)基因7(ATG7)是涉及自噬激活的關(guān)鍵基因,。從機(jī)制上講,,抑制休眠乳腺癌細(xì)胞中的自噬通路導(dǎo)致?lián)p傷線粒體及活性氧的富集,從而導(dǎo)致了癌細(xì)胞凋亡,。
【2】Diabetes:IL-6可通過自噬和抗氧化應(yīng)答保護(hù)β細(xì)胞
doi:10.2337/db17-1280
*,,細(xì)胞在耗氧代謝過程中會產(chǎn)生一系列活性氧簇(ROS),而ROS能夠通過細(xì)胞的氧化應(yīng)激反應(yīng)誘導(dǎo)細(xì)胞凋亡甚至導(dǎo)致細(xì)胞壞死,。之前研究表明活性氧簇(ROS)的產(chǎn)生也是糖尿病中導(dǎo)致β細(xì)胞功能失調(diào)的關(guān)鍵因素,。細(xì)胞因子IL-6曾被發(fā)現(xiàn)與β細(xì)胞自噬存在關(guān)聯(lián),但是在β細(xì)胞抗氧化應(yīng)答情況下的作用還沒有得到研究,。zui近來自印第安納大學(xué)醫(yī)學(xué)院的研究人員發(fā)現(xiàn)IL-6能夠?qū)⒓?xì)胞自噬和抗氧化應(yīng)答在一起影響β細(xì)胞存活,。相關(guān)研究結(jié)果發(fā)表在學(xué)術(shù)期刊Diabetes上。
在這項(xiàng)研究中,,研究人員通過動物模型和培養(yǎng)的人胰島以及小鼠β細(xì)胞來研究IL-6如何影響抗氧化應(yīng)答,。他們發(fā)現(xiàn)IL-6能夠?qū)⒆允珊涂寡趸瘧?yīng)答在一起降低β細(xì)胞和人胰島細(xì)胞的ROS水平。在β細(xì)胞中特異性敲除IL-6會導(dǎo)致敲除小鼠小鼠更容易受到β細(xì)胞特異性毒性物質(zhì)鏈脲霉素和四氧嘧啶造成的氧化損傷和細(xì)胞死亡,。
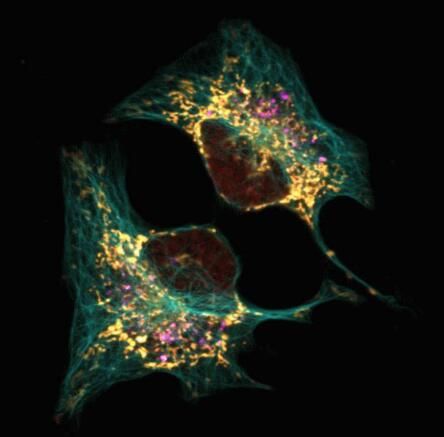
【3】Devel Cell:關(guān)閉細(xì)胞自噬作用或能幫助化療等療法有效殺滅癌細(xì)胞
doi:10.1016/j.devcel.2018.02.014
一種名為細(xì)胞自噬(autophagy)的過程能夠幫助細(xì)胞在壓力下存活,,其能夠扮演細(xì)胞中的再循環(huán)系統(tǒng)來幫助降解并再利用細(xì)胞中的廢物,從而促進(jìn)細(xì)胞健康存活,;但不幸的是,,癌細(xì)胞通常會攔截細(xì)胞自噬來躲避抗癌藥物對癌細(xì)胞的殺滅作用,這就使得細(xì)胞自噬成為了科學(xué)家們開發(fā)新型抗癌療法的潛在靶點(diǎn),,阻斷自噬就能夠使得癌細(xì)胞無法克服療法造成的壓力,,從而誘發(fā)癌細(xì)胞死亡;實(shí)際上,,目前很多臨床試驗(yàn)都正在檢測自噬抑制劑聯(lián)合化療藥物,、放療或靶向性療法是否能夠有效促進(jìn)癌細(xì)胞進(jìn)入到細(xì)胞凋亡階段,。
目前研究人員已經(jīng)清楚細(xì)胞自噬和細(xì)胞凋亡之間的關(guān)聯(lián),但他們并不清楚到底是誰締造了這種關(guān)聯(lián),;換句話說,,研究者知道,關(guān)閉細(xì)胞自噬能夠幫助藥物促進(jìn)癌細(xì)胞發(fā)生凋亡/死亡,,但他們并不知道該過程發(fā)生的具體分子機(jī)制,。近日,一項(xiàng)刊登在雜志Developmental Cell上的研究報(bào)告中,,來自科羅拉多大學(xué)癌癥研究中心的研究人員通過研究發(fā)現(xiàn)了一種名為FOXO3a的轉(zhuǎn)錄因子,,其能將細(xì)胞自噬與細(xì)胞凋亡起來。
【4】Hepatology:中國臺灣學(xué)者發(fā)現(xiàn)增強(qiáng)自噬可有效抑制肝癌
doi:10.1002/hep.29781
細(xì)胞內(nèi)分子降解機(jī)制的紊亂會引起癌癥,,其中包括肝細(xì)胞癌(HCC),。之前研究曾報(bào)道細(xì)胞周期調(diào)控蛋白Cyclin D1在肝細(xì)胞癌中存在過表達(dá);細(xì)胞自噬可以招募和降解具有癌基因作用的miR-224來防止HCC的發(fā)生,,但在HCC發(fā)生過程中Cyclin D1是否也能夠被自噬選擇性降解還不清楚,。
在zui近發(fā)表在學(xué)術(shù)期刊Hepatology上的一項(xiàng)研究中,來自中國臺灣的學(xué)者們在147名HCC病人和3個(gè)小鼠模型的腫瘤中發(fā)現(xiàn)自噬的低活性和Cyclin D1的高表達(dá)存在相關(guān)性,,這些結(jié)果也共同揭示了這兩個(gè)事件與HCC病人的不良生存率存在關(guān)聯(lián),,表明自噬活性和Cyclin D1的表達(dá)在HCC發(fā)展過程中可能有重要作用。
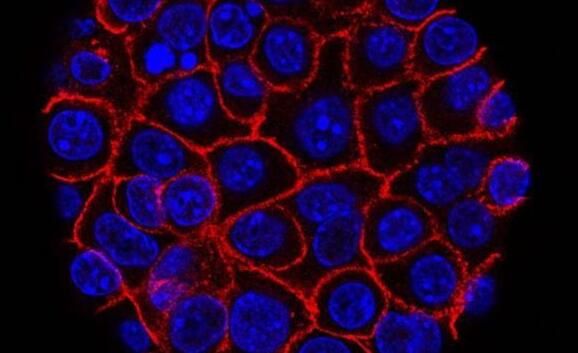
【5】Mol Cell:浙大劉偉組揭示調(diào)控自噬起始和脂質(zhì)生成的新通路
乙?;鳛椴溉閯游锛?xì)胞內(nèi)重要的蛋白翻譯后修飾,,參與調(diào)控眾多的生物學(xué)過程。組蛋白乙酰轉(zhuǎn)移酶p300通過乙?;M蛋白和其他蛋白調(diào)控細(xì)胞的生長和增殖,。然而,我們對細(xì)胞內(nèi)p300的活性調(diào)控機(jī)制卻知之甚少,。10月12日,,Molecular Cell雜志在線發(fā)表來自浙江大學(xué)醫(yī)學(xué)院劉偉教授課題組題為“mTORC1 Phosphorylates Acetyltransferase p300 to Regulate Autophagy and Lipogenesis”的研究論文,該研究發(fā)現(xiàn)調(diào)控細(xì)胞生長和代謝的重要蛋白復(fù)合物mTORC1通過磷酸化p300,,解除p300的分子內(nèi)抑制作用(Intra-molecular inhibition),,促進(jìn)p300的激活。
功能研究發(fā)現(xiàn),,mTORC1-p300通路在自噬起始和脂質(zhì)生成的過程中發(fā)揮重要調(diào)控作用,,提示該通路在協(xié)調(diào)細(xì)胞內(nèi)分解代謝和合成代謝過程中扮演關(guān)鍵角色。蛋白的乙?;瘏⑴c調(diào)控細(xì)胞代謝的眾多環(huán)節(jié),,提示乙酰轉(zhuǎn)移酶/去乙酰化酶在細(xì)胞代謝調(diào)節(jié)中發(fā)揮重要作用,。作為細(xì)胞內(nèi)重要的乙酰轉(zhuǎn)移酶,,p300和其同源蛋白CBP,,zui早發(fā)現(xiàn)在細(xì)胞核內(nèi)通過乙酰化組蛋白和轉(zhuǎn)錄因子,,充當(dāng)轉(zhuǎn)錄共激活子(coactivator),,調(diào)控基因轉(zhuǎn)錄。p300也可以通過乙?;?xì)胞質(zhì)中的蛋白,,參與調(diào)控細(xì)胞質(zhì)中的生物學(xué)過程。zui近的研究發(fā)現(xiàn),,p300在細(xì)胞內(nèi)重要的分解代謝過程自噬中發(fā)揮調(diào)控作用。p300通過乙?;允上嚓P(guān)蛋白LC3,,Atg5和Atg7抑制自噬的起始。葡萄糖饑餓時(shí),,這些蛋白的去乙?;窼irt1被AMPK激活,誘導(dǎo)自噬相關(guān)蛋白去乙?;?,促進(jìn)自噬的發(fā)生。
【6】解密“自噬”,,抗癌治病更近一步
日本科學(xué)家大隅良典因發(fā)現(xiàn)細(xì)胞自噬的分子機(jī)制獲得2016年諾貝爾生理學(xué)或醫(yī)學(xué)獎(jiǎng),。
統(tǒng)計(jì)顯示,每天我國都有7000多人死于癌癥,。但直到現(xiàn)在,,癌癥的發(fā)病機(jī)制仍然待解。
自上世紀(jì)60年代科學(xué)家發(fā)現(xiàn)細(xì)胞自噬現(xiàn)象以來,,人們獲知衰老,、癌癥可能與我們身體的zui小組成單位——細(xì)胞受損有關(guān),但其詳細(xì)機(jī)制如何,,一直未有定論,。這一生命之謎陷入長久僵局。
50多年后,,日本科學(xué)家大隅良典開創(chuàng)性地發(fā)現(xiàn)了細(xì)胞自噬的分子機(jī)制和生理功能,,為闡明細(xì)胞受損的詳細(xì)機(jī)制鋪平了道路。這一突破性研究,,不僅讓他摘得2016年諾貝爾生理學(xué)或醫(yī)學(xué)獎(jiǎng),,更為人類防治癌癥、帕金森,、心血管病等疾病,,甚至延緩衰老打開了一扇新的大門,。
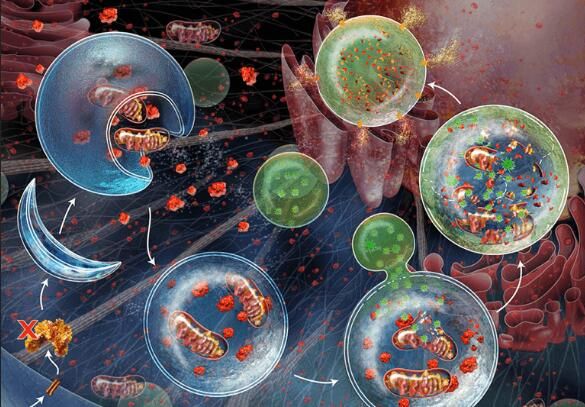
【7】Nat Commun:揭示自噬功能障礙導(dǎo)致炎癥和腸道疾病機(jī)制
doi:10.1038/s41467-017-01287-9
自噬是一種常見的至關(guān)重要的細(xì)胞過程。細(xì)胞通過自噬在其內(nèi)部降解和循環(huán)利用有害的或受損的組分,,從而讓我們的身體保持健康,。
在一項(xiàng)新的研究中,英國華威大學(xué)生命科學(xué)學(xué)院的Ioannis Nezis博士和同事們揭示出炎癥與自噬存在新的關(guān)聯(lián),。他們證實(shí)自噬存在功能故障會導(dǎo)致組織炎癥,,從而讓人更容易患上有害的疾病,特別是腸道疾病,。這一發(fā)現(xiàn)可能更好地治療,,甚至預(yù)防結(jié)腸癌、克羅恩病和其他的腸道疾病,。相關(guān)研究結(jié)果于2017年11月2日在線發(fā)表在Nature Communications期刊上,,論文標(biāo)題為“Kenny mediates selective autophagic degradation of the IKK complex to control innate immune responses”。
理解這種關(guān)聯(lián)可能導(dǎo)致人們開發(fā)出更加有效的方法來治療腸道疾病,,如結(jié)腸癌,、腸易激綜合征、克羅恩病和潰瘍性結(jié)腸炎,,從而讓醫(yī)療專業(yè)人員能夠通過調(diào)節(jié)和控制自噬來靶向這些疾病的根源,。
【8】Nature子刊揭示:自噬紊亂易引發(fā)腸道疾病
發(fā)表在Nature Communications上的一篇研究報(bào)告中,研究人員通過研究將炎癥與一種基本的生物學(xué)過程—自噬關(guān)聯(lián)了起來,,并構(gòu)建了一種新關(guān)系,,用于防治包括結(jié)腸癌、克羅恩病,、潰瘍性結(jié)腸炎在內(nèi)的腸道疾病,。
自噬,是一種“自己吃自己”過程,,是細(xì)胞維持物質(zhì)周轉(zhuǎn)的重要機(jī)制,。當(dāng)細(xì)胞內(nèi)出現(xiàn)衰老的蛋白質(zhì)、損壞的細(xì)胞器等廢棄物時(shí),,自噬囊泡會將它們包裹并送至溶酶體中進(jìn)行降解并得以循環(huán)利用,,從而確保細(xì)胞自身本身的代謝需要和某些細(xì)胞器的更新。
近期,,來自于華威大學(xué)生命科學(xué)學(xué)院的Ioannis P. Nezis教授帶領(lǐng)團(tuán)隊(duì)發(fā)現(xiàn):當(dāng)自噬功能紊亂時(shí),,會引發(fā)炎癥,從而增加腸道疾病的發(fā)生風(fēng)險(xiǎn),。他們以果蠅為模型,,發(fā)現(xiàn)了一個(gè)調(diào)控自噬的關(guān)鍵蛋白——Kenny。這一蛋白質(zhì)含有一個(gè)motif,是啟動蛋白“自噬分解”的關(guān)鍵元件,。當(dāng)自噬功能失調(diào)時(shí),,Kenny會聚集并引發(fā)炎癥。
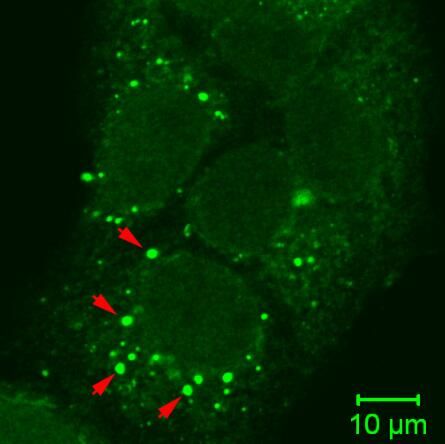
【9】Immunity:自噬如何影響免疫又添新證據(jù)
doi:10.1016/j.immuni.2017.08.005
嗜中性粒細(xì)胞是非常重要但壽命短暫的一類免疫細(xì)胞,,而作為固有免疫的介導(dǎo)者需要不斷補(bǔ)充這類細(xì)胞,。嗜中性粒細(xì)胞在骨髓中的分化需要各種細(xì)胞質(zhì)和細(xì)胞核內(nèi)的重塑過程,這些變化的發(fā)生需要細(xì)胞提供大量能量,,但是其中的能量調(diào)解過程仍然不為人知,。雖然之前有研究表明自噬對于其它血細(xì)胞譜系的分化有重要作用,但是在粒細(xì)胞生成過程中的作用也仍然不清楚,。
在這項(xiàng)發(fā)表在學(xué)術(shù)期刊Immunity上的新研究中,,來自牛津大學(xué)的科學(xué)家們發(fā)現(xiàn)代謝和自噬會隨發(fā)育過程進(jìn)行運(yùn)行并且對體內(nèi)嗜中性粒細(xì)胞的分化非常重要。缺失了Atg7的嗜中性粒細(xì)胞前體細(xì)胞有更強(qiáng)的糖酵解活性但是線粒體呼吸受到損傷,,ATP合成下降同時(shí)會積累脂滴,。
【10】Cancer Res:自噬抑制劑對治療黑色素瘤是否有效還需關(guān)注另一因素
doi:10.1158/0008-5472.CAN-17-0907
細(xì)胞自噬是參與維持細(xì)胞內(nèi)穩(wěn)態(tài)的一個(gè)分解代謝過程,能夠降解一些細(xì)胞成分為新分子的合成提供基本的原料,。許多研究發(fā)現(xiàn)自噬是與癌細(xì)胞存活有關(guān)的一個(gè)關(guān)鍵特征,,因此通過改變自噬過程促進(jìn)細(xì)胞死亡獲得了許多科學(xué)家的關(guān)注,。
自噬介導(dǎo)了癌細(xì)胞對多種抗癌藥物的抵抗,,而對于黑色素瘤來說,癌細(xì)胞對靶向治療的抵抗還與Wnt的表達(dá)有關(guān),,Wnt是抑制經(jīng)典Wnt信號通路關(guān)鍵分子β-catenin表達(dá)的一個(gè)內(nèi)在因子,,也能夠促進(jìn)腫瘤的侵襲。鑒于這兩個(gè)因素都能夠引起癌細(xì)胞對抗癌藥物的抵抗,,深入了解兩者之間的內(nèi)在關(guān)系對于黑色素瘤治療和解決耐藥性問題都有比較重要的意義,。
zui近來自美國費(fèi)城Wistar研究所的Ashani T. Weeraratna教授帶領(lǐng)研究人員對黑色素瘤中Wnt和細(xì)胞自噬的內(nèi)在關(guān)系進(jìn)行了深入分析,并將相關(guān)研究結(jié)果在線發(fā)表在學(xué)術(shù)期刊Cancer Research上,。(生物谷)
 您好, 歡迎來到化工儀器網(wǎng)
您好, 歡迎來到化工儀器網(wǎng)

 12
12


