齊瑤
研究難點
病毒是一種個體微小、結(jié)構(gòu)簡單,、只含一種核酸(DNA或RNA),、必須在活細胞內(nèi)寄生并以復(fù)制方式增殖的非細胞型生物,。而病毒侵染宿主細胞卻是一個非常復(fù)雜的過程,主要分為吸附(Attachment),、進入(Entry/Penetration),、復(fù)制(Replication)、大分子合成(Biosynthesis),、裝配(Assembly),、釋放(Release)等幾個階段,如圖1,。
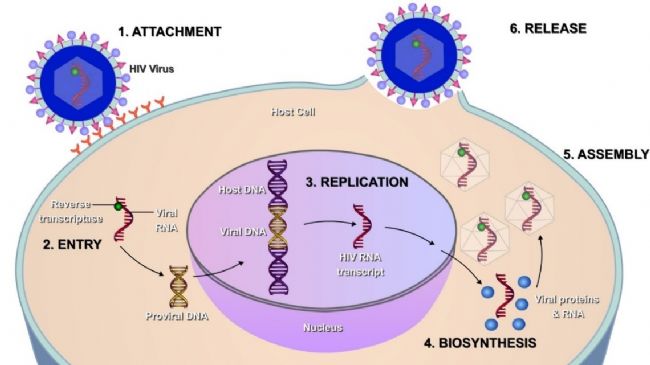
圖1.HIV病毒侵染人源細胞過程示意圖[1]
如何從初始的吸附和進入階段進行干預(yù)阻斷,,是病毒性疾病防治的切入點之一。以人類免疫缺陷病毒(HIV),,也就是引發(fā)艾滋病的病原為例,,它通過顆粒表面的包膜糖蛋白(Env)與免疫細胞表面的CD4分子、輔助受體互作,,實現(xiàn)病毒與宿主細胞的融合,、感染過程??茖W(xué)家們曾運用BlaM(β-內(nèi)酰胺酶分析:測量細胞群中病毒融合的技術(shù))或細胞內(nèi)病毒衣殼蛋白p24分析等多種方法對病毒的侵染過程進行檢測,,但由于技術(shù)的限制,均不能直接實時監(jiān)測病毒進入宿主細胞的動態(tài)融合過程[2],。因此,,在時間和空間上都具備高靈敏度的FLIM-FRET,成為了該項研究的破冰技術(shù),。
FLIM-FRET
經(jīng)常關(guān)注徠卡課堂的同學(xué)們,,想必對FLIM-FRET都不陌生了。在這里,,我們再簡單回顧一下幾個關(guān)鍵性的概念,。
熒光壽命:熒光是指熒光分子吸收能量后,其處于基態(tài)(S0)的電子躍遷至激發(fā)態(tài)(S1),,經(jīng)過短暫停留,,由激發(fā)態(tài)(S1)再回到基態(tài)(S0)時釋放出光的現(xiàn)象,而熒光分子停留在激發(fā)態(tài)的時間就是熒光壽命(圖2A),。與熒光光譜一樣,,熒光壽命也是熒光物質(zhì)的一種內(nèi)在*性質(zhì)。
FLIM(Fluorescence Lifetime Imaging,,熒光壽命成像):是一種基于熒光壽命的顯微成像技術(shù),,其成像結(jié)果提供像素位點的壽命信息(如圖2B),使得我們在熒光強度成像之外,,能更加深入地對樣品進行功能性測量,。熒光壽命成像具有不同于熒光強度成像的眾多優(yōu)點,,如不受熒光物質(zhì)濃度、光漂白,、激發(fā)光強度等因素的影響,。但會因為分子構(gòu)象、分子間相互作用,、分子微環(huán)境,、生理狀態(tài)等條件改變而發(fā)生變化,因此熒光壽命可用于分析分子的這些變化,,基于熒光壽命測量的FRET是FLIM的重要應(yīng)用之一,。
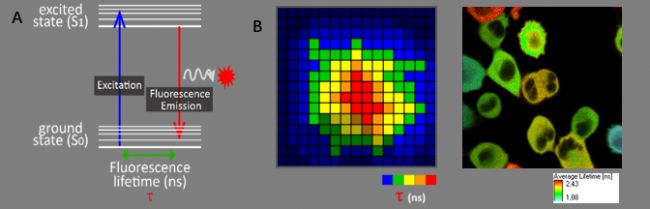
圖2. A. 熒光壽命示意圖;B. FLIM:提供每個像素位點的熒光壽命信息(左),;基于熒光壽命信息的細胞成像結(jié)果(右)
FRET(Fluorescence Resonance Energy Transfer,,熒光共振能量轉(zhuǎn)移):供體熒光基團(Donor)的發(fā)射光譜與受體熒光基團(Acceptor)的吸收光譜有一定的重疊,當供體被激發(fā)后,,且兩個熒光基團間的距離小于10nm時,,處于激發(fā)態(tài)的供體將把一部分或全部能量轉(zhuǎn)移給受體,使受體被激發(fā),,即發(fā)生熒光能量的非放射性轉(zhuǎn)移現(xiàn)象,,為FRET(如圖3),這一過程也伴隨著供體熒光壽命的縮短和受體熒光壽命的延長,。
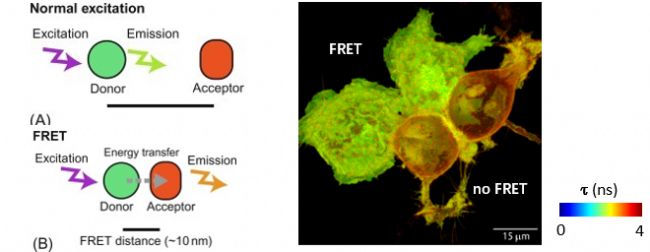 圖3. FRET原理(左)[2]及FRET實例(右)
圖3. FRET原理(左)[2]及FRET實例(右)
(右):用FLIM-FRET測量N1E-115 細胞膜上PH結(jié)構(gòu)域的相互作用,,發(fā)生FRET的細胞呈現(xiàn)較短的熒光壽命(偏綠),未發(fā)生FRET的細胞呈現(xiàn)較長的熒光壽命(偏紅)
FLIM-FRET兼具 FLIM 和 FRET 兩者的優(yōu)勢,,不受熒光物質(zhì)濃度,、光漂白、激發(fā)光強度等因素的影響,,且樣品制備簡單,測量結(jié)果準確性高,,易重復(fù),。因此,F(xiàn)LIM-FRET非常適合于進行分子間相互作用,、分子構(gòu)象或生理狀態(tài)改變等的研究,。
應(yīng)用實例
那么科學(xué)家是如何將FLIM-FRET應(yīng)用于監(jiān)測HIV病毒侵入宿主細胞的動態(tài)過程呢,讓我們看以下兩個實例:
(一)利用FRET生物傳感器示蹤HIV進入宿主細胞過程[3]來自牛津大學(xué)的研究者設(shè)計了一個HIV-Chameleon生物傳感器,,由一對能夠發(fā)生FRET的熒光團(mTFP1和eYFP)組成,,兩個熒光團之間通過短肽序列(包含煙草蝕刻病毒TEV蛋白酶切割位點)鏈接在一起(如圖4A右)。TEV蛋白酶(TEVp)可以與HIV-1 Vpr蛋白或Gag蛋白融合,,摻入病毒顆粒中,。當包含TEV蛋白酶的病毒與表達生物傳感器的細胞融合時,,Vpr-TEV或Gag-TEV(rTEV)被釋放到細胞質(zhì)中,并特異性地裂解鏈接序列,,增加mTFP1與eYFP之間距離至10nm以上,,阻斷FRET,并可通過FLIM進行測量,。圖4B為FLIM偽彩圖與圖像中所有像素的壽命直方圖,,其中藍色表示較短的壽命(無融合),紅色表示較長的壽命(融合),。這樣就可以實時定量熒光壽命的改變,,從而示蹤病毒與宿主細胞融合的瞬間動態(tài)過程。作者將所得結(jié)果與廣泛使用的BlaM分析結(jié)果比對,,二者具有高度匹配性,,因此,HIV-Chameleon生物傳感器與FRET-FLIM的結(jié)合使用,,可以實現(xiàn)單個活細胞或群體的病毒融合動力學(xué)實時監(jiān)測,。
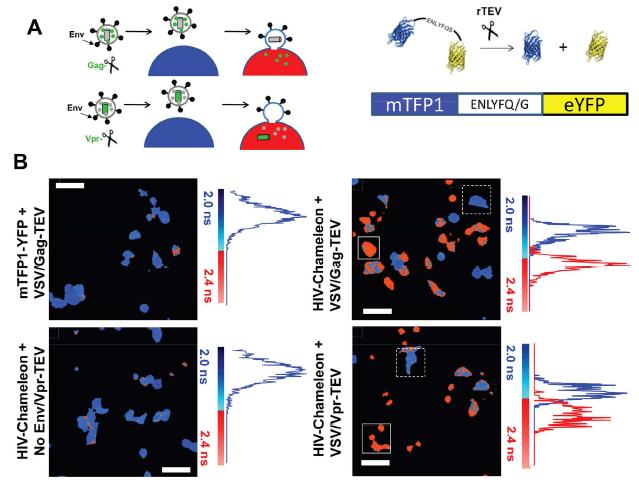 圖4. HIV-Chameleon檢測病毒融合[3]
圖4. HIV-Chameleon檢測病毒融合[3]
A.(左)TEV蛋白酶(TEVp)與HIV-1 Vpr蛋白或Gag蛋白融合的兩種包裝過程;(右)HIV-Chameleon生物傳感器示意圖,;B.病毒融合前后的熒光壽命成像(Scale Bar=30μm)
(二)細胞代謝水平對于HIV-1侵染宿主細胞的影響[4]研究人員在HIV-1病毒的侵染機制研究中發(fā)現(xiàn),,病毒侵染過程中,宿主細胞代謝水平與膜狀態(tài)改變有關(guān),。將FRET生物傳感器瞬時轉(zhuǎn)染到細胞中(如圖5A),,記錄瞬時表達這些生物傳感器的細胞的FLIM圖像,并進行BlaM分析,,結(jié)果表明,,乳酸濃度較高的單細胞與病毒融合性更高,此外,,具有更高ATP/ADP比率的細胞與病毒的融合性更高(如圖5B),。也就是說,糖酵解通量較高的細胞更容易被HIV-1感染,。
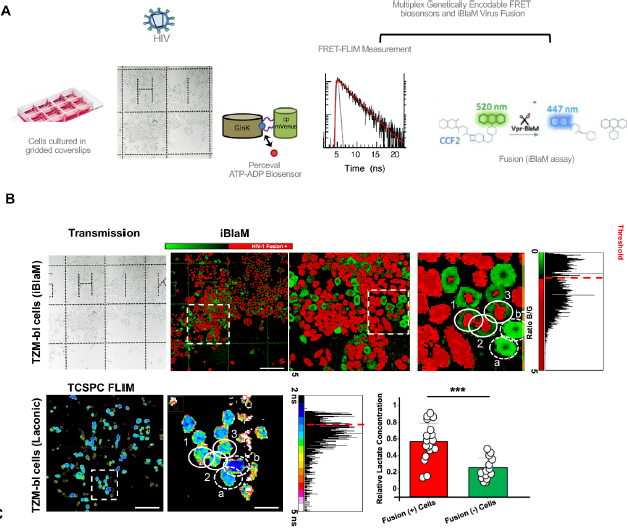
圖5. 單個細胞中的相對乳酸濃度和ATP / ADP比率與HIV-1融合相關(guān)[4],;
(A)FRET生物傳感器;(B)同樣區(qū)域細胞的BlaM(上)和FLIM成像(下),白色實線所示為正在與病毒融合的細胞,,在BlaM中呈紅色,,熒光壽命較長,白色虛線所示為未融合的細胞,,BlaM中呈綠色,,熒光壽命較短
進一步的分析表明,2-脫氧-d-葡萄糖(2-DG)對糖酵解的靶向抑制作用大大降低了HIV-1的融合和感染。而用2-DG處理的細胞分別具有較低的膜膽固醇和較高的膜張力值,。因此,,作者構(gòu)建了一種基于Ypet/eCFP FRET的膜張力感應(yīng)器MSS,由一個彈性張力傳感模塊和兩個與脂分子連接的蛋白質(zhì)組成,,這兩個蛋白質(zhì)錨定在質(zhì)膜的Raft和非Raft區(qū)域,,對膜張力變化非常敏感(如圖6)。通過FLIM測量單個細胞MSS張力探針瞬時表達,,證實了HIV-1需要在膜張力較低的區(qū)域進入細胞,,也進一步確定了宿主細胞糖酵解活性和膜張力之間的聯(lián)系,其在活細胞中的單病毒融合水平上實時影響HIV-1融合,。
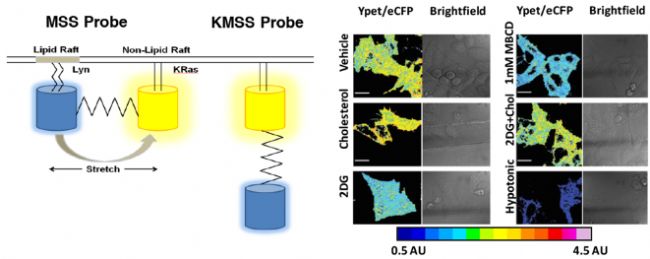 圖6.(左)靈敏型膜張力感應(yīng)器MSS探針以及對照組非靈敏型感應(yīng)器KMSS探針示意圖,;(右)多種不同處理條件下,TZM-bl 細胞表達MSS的FRET效率成像[4]
圖6.(左)靈敏型膜張力感應(yīng)器MSS探針以及對照組非靈敏型感應(yīng)器KMSS探針示意圖,;(右)多種不同處理條件下,TZM-bl 細胞表達MSS的FRET效率成像[4]
總結(jié)
FLIM-FRET提供了基于群體方法或光譜方法所難以實現(xiàn)的單細胞微環(huán)境中的分辨率,,能以高時空分辨率在單個細胞中可視化和識別影響HIV-1感染的關(guān)鍵因素,,實現(xiàn)單一病毒跟蹤技術(shù)。這對于在HIV-1感染早期階段尋找艾滋病的治療方法,,有著重要的科學(xué)意義,。
創(chuàng)新、高效的技術(shù)和設(shè)備,,是科研工作者們揭示生命奧義的得力工具,,也是在面對新型突發(fā)病毒時的尖兵利器。Leica全新 STELLARIS 8 FALCON熒光壽命成像系統(tǒng),,搭載新一代白激光(440-790nm)以及HyD X高靈敏度專用檢測器,,提供超快速、多維度熒光壽命成像解決方案,。想了解更多關(guān)于Leica STELLARIS 8 FALCON產(chǎn)品信息或病毒的研究方法,,敬請關(guān)注徠卡的Wx公眾號“徠卡顯微系統(tǒng)”,我們下期再見,。
立即詢價
您提交后,專屬客服將第一時間為您服務(wù)