單抗藥物如何攻克阿爾茨海默癥 靶點(diǎn)大揭秘_MedChemExpress(MCE 中國(guó))

老年癡呆!它還有個(gè)洋氣的名字——阿爾茨海默癥,。一種常見(jiàn)的神經(jīng)退行性疾病,,病理現(xiàn)象主要涉及 β-淀粉樣蛋白斑塊、神經(jīng)纖維纏結(jié),、神經(jīng)元喪失和炎癥反應(yīng)等,。近年來(lái),其對(duì)應(yīng)靶點(diǎn)的治療藥物也層出不窮……
Aducanumab 在 2021 年 6 月 7 日獲得 FDA 加速批準(zhǔn)上市,,是第一個(gè)被 FDA 批準(zhǔn)用于 AD 的新藥,,用于 AD 源性輕度認(rèn)知障礙 (MCI) 及輕度 AD 的治療。2023 年 1 月 6 日,,F(xiàn)DA 批準(zhǔn) Lecanemab 上市,,用于治療伴有輕度認(rèn)知功能障礙或輕度癡呆的早期 AD。這標(biāo)志著利用單抗藥物作為阿爾茨海默癥治療手段的可行性得到了認(rèn)可,。
本期小 M 就為大家盤點(diǎn)下都有哪些治療阿爾茨海默癥的單抗藥物,!
Section.01
靶向 β-淀粉樣蛋白 (Aβ) 的
單抗藥物
淀粉樣蛋白前體蛋白 (APPs) 是天然存在于大多數(shù)組織中的跨膜蛋白。α-分泌酶將 APP 裂解成可溶性肽,。然而,,通過(guò) β 分泌酶和隨后的 γ 分泌酶,產(chǎn)生淀粉樣蛋白 β 單體 Aβ1-40 和 Aβ1-42,,然后形成低聚物和大聚合物,。β 淀粉樣蛋白以多種形式存在,例如單體,、寡聚體,、原纖維和原纖維。寡聚體和原纖維具有神經(jīng)毒性,。淀粉樣蛋白級(jí)聯(lián)假說(shuō) (ACH) 規(guī)定,,越來(lái)越多的聚集細(xì)胞外 Aβ,特別是可溶性寡聚物,,具有神經(jīng)毒性,,促進(jìn) tau 蛋白分解,并形成神經(jīng)原纖維纏結(jié),。這導(dǎo)致神經(jīng)元死亡,,表現(xiàn)為臨床前疾病,最終發(fā)展為阿爾茨海默癥,。
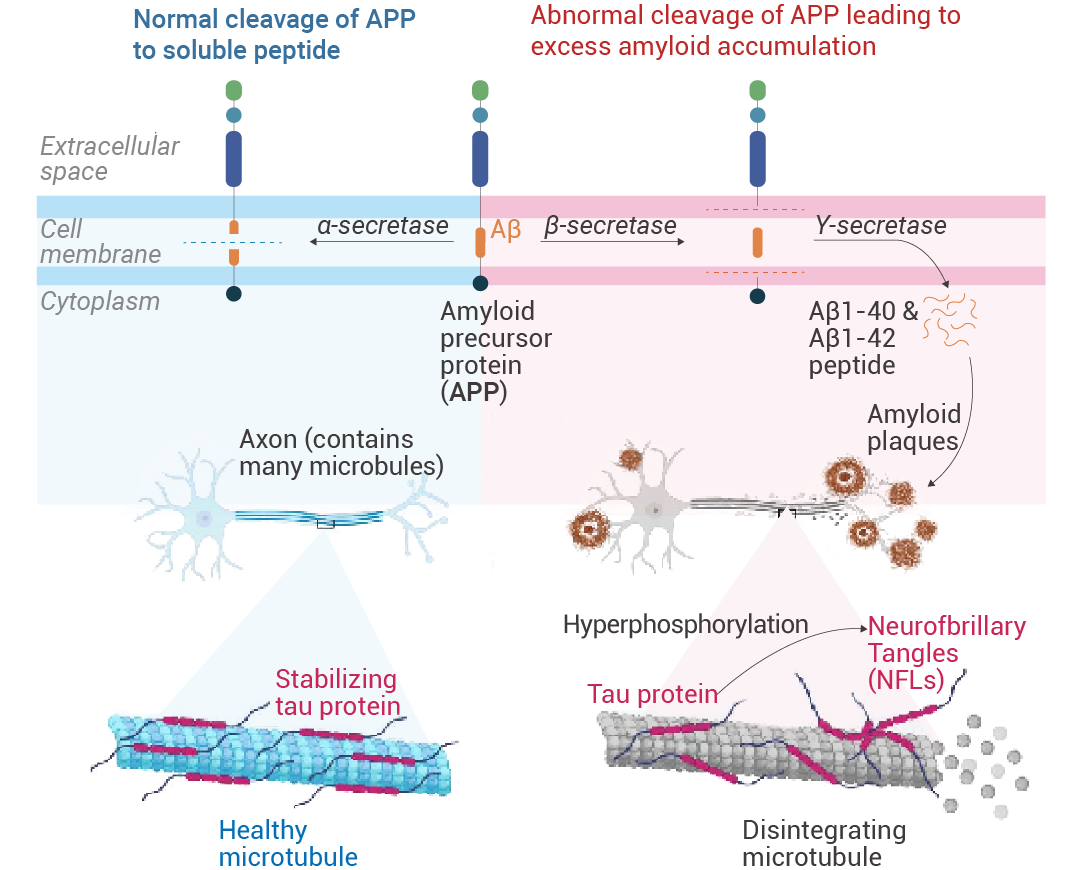
圖 1. 阿爾茨海默癥的病理生理學(xué)[1],。
Aducanumab (阿杜那單抗) 是一種高親和力、靶向- Aβ 構(gòu)象表位的全人 IgG1 單克隆抗體,。它能夠有選擇性地與 AD 患者大腦中的淀粉樣蛋白沉積結(jié)合,,然后通過(guò)激活免疫系統(tǒng),將大腦中的沉積蛋白清除。
Aducanumab 于 2021 年 6 月在美國(guó)獲 FDA 批準(zhǔn)上市,,是自 2003 年以來(lái)獲批用于治療阿爾茨海默癥的新療法,。在臨床前研究中,Aducanumab 可以穿透血腦屏障,,靶向淀粉樣斑塊并將其從轉(zhuǎn)基因小鼠大腦中清除,。Aducanumab 臨床研究在 3,482 名阿爾茨海默病患者中進(jìn)行,分為三項(xiàng)獨(dú)立的研究,,包括雙盲,、安慰劑對(duì)照、隨機(jī)和劑量范圍方式,。臨床評(píng)估結(jié)果表明,,接受治療的患者 Aβ-淀粉樣蛋白在劑量和時(shí)間依賴性方面顯著減少,而對(duì)照組患者的 Aβ-淀粉樣蛋白斑塊沒(méi)有減少,。
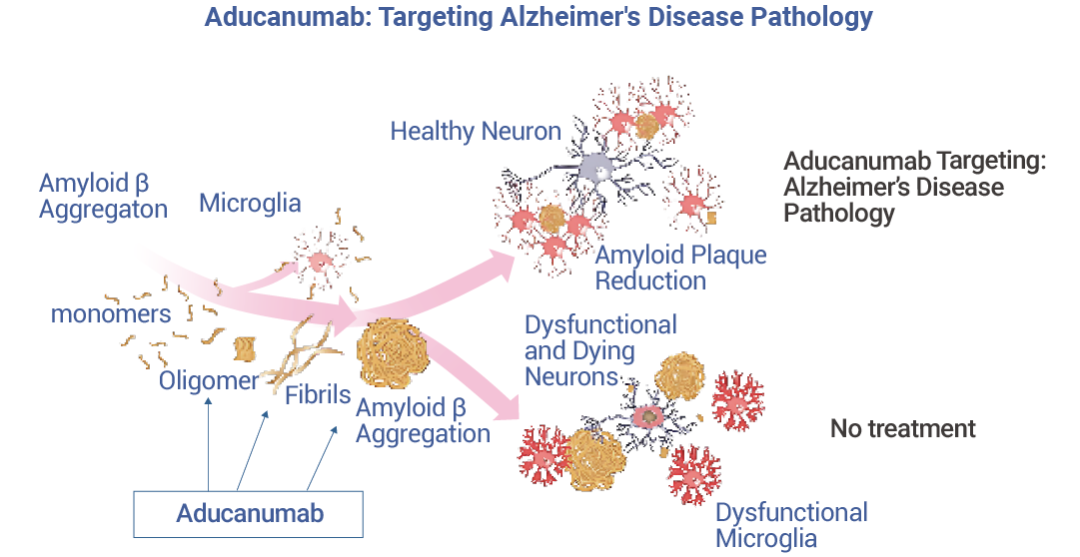
圖 2. Aducanumab 的作用機(jī)制[2],。
Lecanemab (侖卡奈單抗) 是鼠抗體 mAb158 的人源化 IgG1 形式,已被證明可降低致病性 Aβ,,防止 Aβ 沉積,,并特異性地減少 AD 動(dòng)物模型中大腦和 CSF 中的 Aβ 原纖維。Aβ 原纖維的選擇性靶標(biāo)將 Lecanemab 與其他抗淀粉樣蛋白 mAb 區(qū)分開(kāi)來(lái),。Lecanemab 是有效的第二代單克隆抗體,,用于免疫耗竭 Aβ 原纖維,尤其是可溶性原纖維和寡聚體,。Lecanemab 結(jié)合可溶性原纖維的親和力是 Aducanumab 的 100 倍,,與不溶性原纖維的親和力是 25 倍,對(duì)單體的結(jié)合親和力較低,。2023 年 7 月美國(guó) FDA 全面批準(zhǔn)它用于治療阿爾茨海默病 (AD) 導(dǎo)致的輕度認(rèn)知功能損害和早期癡呆,。
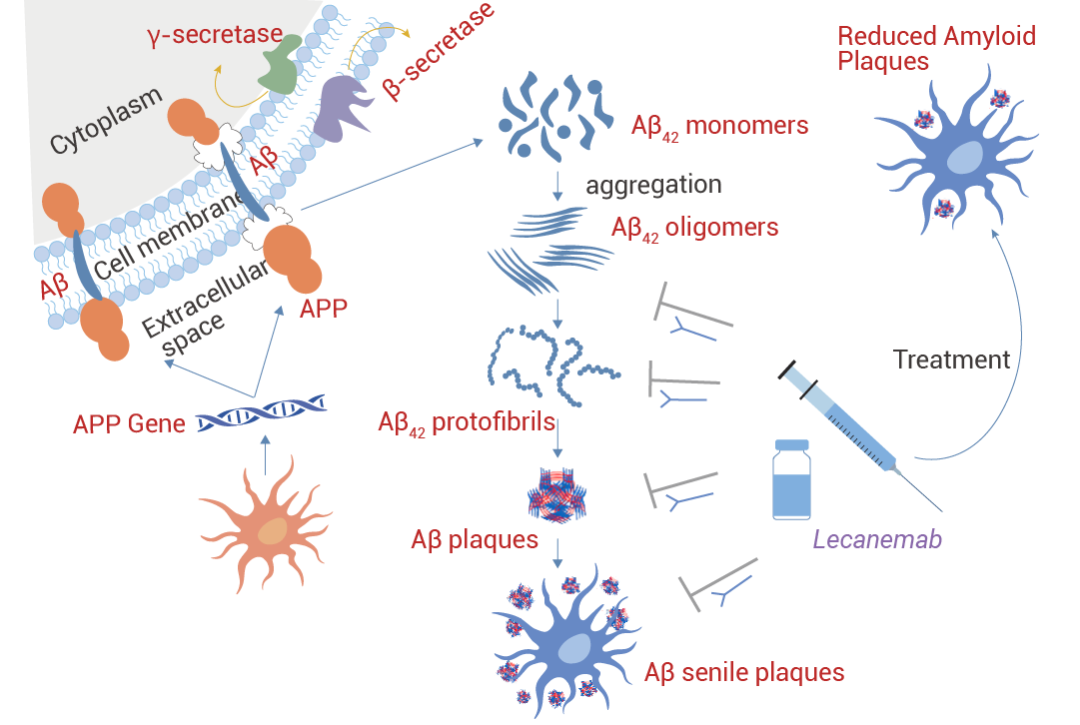
圖 3. Lecanemab 的作用機(jī)制[3]。
Donanemab (多奈單抗) 是人源化 IgG1 抗體,,靶向 N 端 Aβ 表位,,并通過(guò)小膠質(zhì)細(xì)胞介導(dǎo)的吞噬作用幫助去除斑塊。Donanemab 的開(kāi)發(fā)旨在通過(guò)小膠質(zhì)細(xì)胞介導(dǎo)的吞噬作用去除現(xiàn)有的淀粉樣蛋白斑塊,。在老年淀粉樣蛋白前體蛋白轉(zhuǎn)基因小鼠中施用 Donanemab 可導(dǎo)致劑量依賴性斑塊減少,,而無(wú)微出血傾向。Donanemab 不與其他 Aβ 物種,、神經(jīng)遞質(zhì)或其受體的脫靶結(jié)合,,并且沒(méi)有已知的癥狀效應(yīng)。
Bapineuzumab (巴匹珠單抗) 是小鼠單克隆抗體 3D6 的人源化形式,,靶向 Aβ 的 N 端區(qū)域,。這種被動(dòng)免疫療法的基本原理是抗體結(jié)合會(huì)清除過(guò)量的 Aβ,。支持 Bapineuzumab 的臨床前研究中,,有很大一部分是通過(guò) 3D6 評(píng)價(jià)的,。研究表明,外周給藥的一小部分抗體進(jìn)入了中樞神經(jīng)系統(tǒng),。該抗體能與淀粉樣蛋白斑塊結(jié)合,,降低斑塊負(fù)荷,改善突觸毒性測(cè)量,,并改善小鼠行為測(cè)定的表現(xiàn),。此外,II 期臨床試驗(yàn)表明,,Bapineuzumab 可以降低正電子發(fā)射斷層掃描 (PET) 上淀粉樣蛋白的負(fù)荷和腦脊液中磷酸化 tau 蛋白的濃度,。
Solanezumab (索拉珠單抗) 是一種針對(duì) Aβ 肽中間結(jié)構(gòu)域的人源化單克隆 IgG1 抗體。它識(shí)別可溶性單體 Aβ,,而不是原纖維 Aβ,。在臨床前研究中,單次注射 M266 (Solanezumab 的小鼠版本) 可逆轉(zhuǎn) APP 轉(zhuǎn)基因小鼠模型中的記憶缺陷,,同時(shí)保留淀粉樣蛋白斑塊,,提高了靶向 Aβ 可溶性庫(kù)的可能性。臨床前阿爾茨海默病患者的 3 期試驗(yàn)中,,Solanezumab 靶向腦淀粉樣蛋白水平升高患者的單體淀粉樣蛋白,。但與安慰劑相比,Solanezumab 在 240 周的時(shí)間內(nèi)并沒(méi)有減緩臨床前阿爾茨海默病患者的認(rèn)知能力下降,。
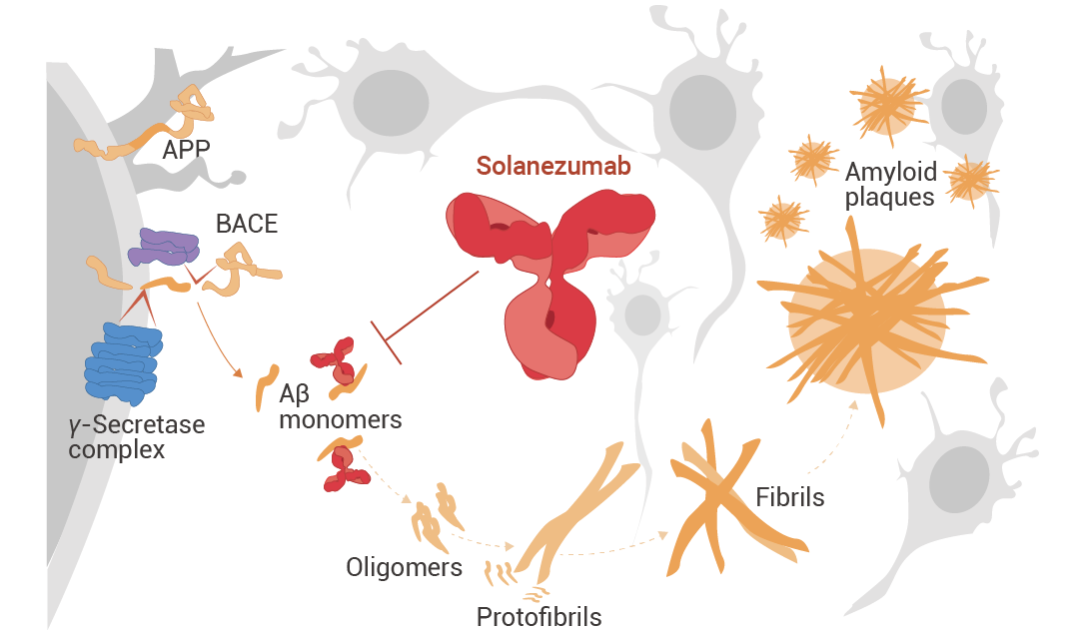
圖 4. Solanezumab 的作用機(jī)制[4],。
Gantenerumab (更汀蘆單抗) 是一種全人源 IgG1 抗體,以亞納摩爾親和力結(jié)合 Aβ 原纖維上的構(gòu)象表位,。它包含 Aβ 的 N 末端和中心氨基酸,。該抗體通過(guò)募集小膠質(zhì)細(xì)胞和激活吞噬作用,集中作用以分解和降解淀粉樣蛋白斑塊,。Gantenerumab 優(yōu)先與聚集的腦 Aβ 相互作用,,包括實(shí)質(zhì)和血管。它還中和寡聚 Aβ42 介導(dǎo)的對(duì)大鼠大腦長(zhǎng)期增強(qiáng)的抑制作用,。在 APP/PS-1 轉(zhuǎn)基因小鼠中,,gantenerumab 與腦 Aβ 結(jié)合,通過(guò)募集小膠質(zhì)細(xì)胞來(lái)減少小斑塊,,并防止新斑塊的形成,。
Crenezumab (克瑞組單抗) 是一種人源化 IgG4 抗體,可識(shí)別多種形式的聚集 Aβ,,包括具有高親和力的寡聚體和原纖維物種,,以及低親和力的單體 Aβ,。與 IgG1 相比,Crenezumab 的 IgG4 骨架賦予減少的 FcγR 激活,,并被證明可以最大限度地減少 FcγR 介導(dǎo)的小膠質(zhì)細(xì)胞炎癥激活,。Crenezumab 刺激淀粉樣蛋白吞噬作用,同時(shí)限制炎性細(xì)胞因子的釋放,,以避免血管源性水腫等副作用,。值得注意的是,Crenezumab 螯合了 Aβ 的疏水核心,,打破了 β-hairpin 構(gòu)象的基本鹽橋特征,,消除了 Aβ 寡聚體和原纖維中基本特征。
Section.02
靶向 tau 蛋白的單抗藥物
tau 是由 352-441 個(gè)氨基酸形成的中樞神經(jīng)系統(tǒng)重要蛋白,,由 17 號(hào)染色體上的 MAPT 基因編碼,,可產(chǎn)生 6 種亞型。tau 的主要功能是促進(jìn)神經(jīng)元軸突中微管的組裝和穩(wěn)定,。tau 與微管的結(jié)合受其磷酸化/去磷酸化平衡的調(diào)節(jié),。在生理?xiàng)l件下,tau 被展開(kāi)和磷酸化,,而病理形式的特征是過(guò)度磷酸化導(dǎo)致從微管脫離,,以及構(gòu)象變化導(dǎo)致形成異常磷酸化 tau 的成對(duì)螺旋和直絲,隨后形成 tau 聚集體,。這些聚集體會(huì)導(dǎo)致神經(jīng)元和神經(jīng)膠質(zhì)細(xì)胞退化,,最終導(dǎo)致各種臨床認(rèn)知、行為和運(yùn)動(dòng)表現(xiàn),,這些表現(xiàn)被歸類為不同類型的神經(jīng)退行性疾病,,稱為 “tau 蛋白病”。
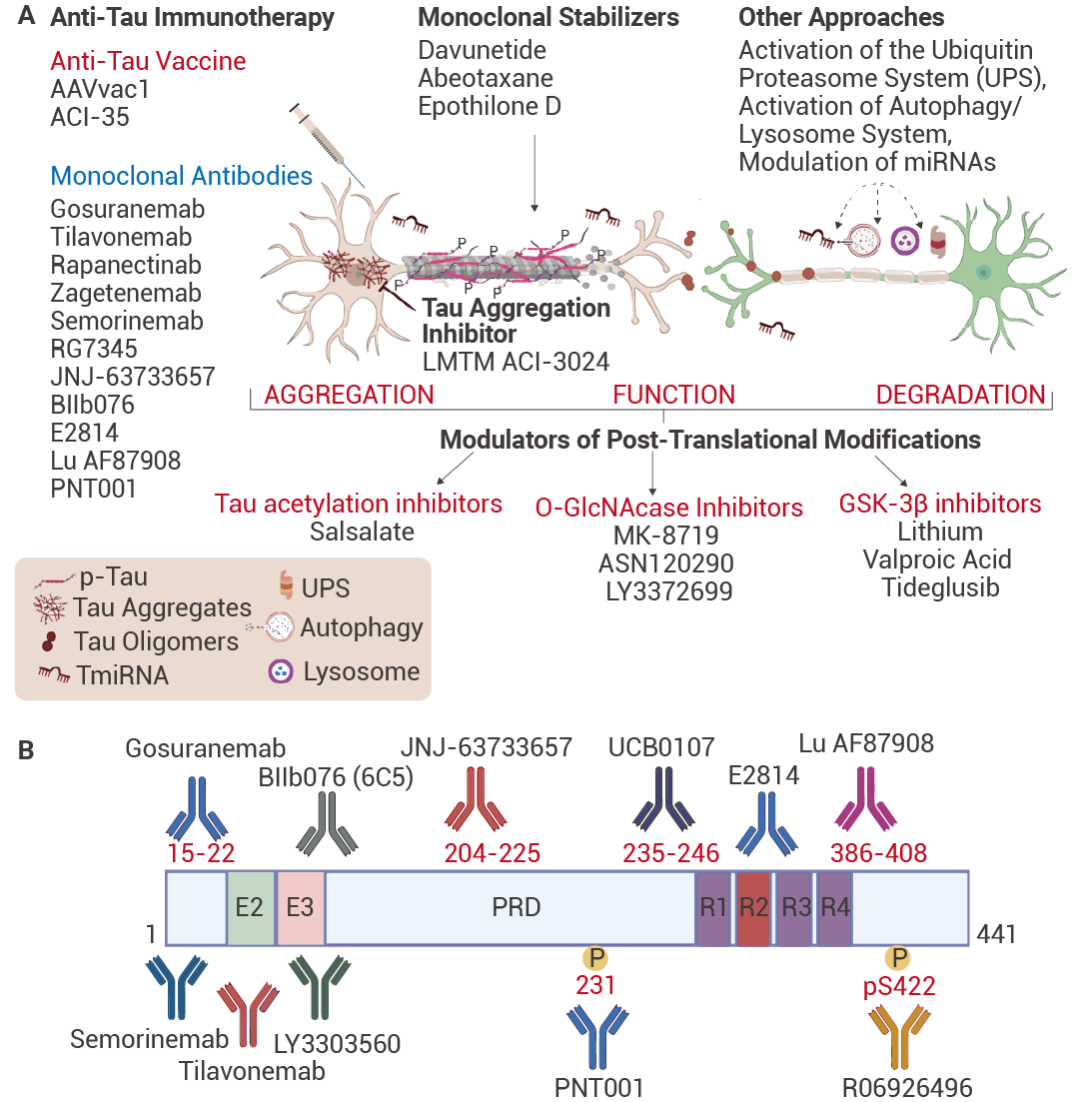
圖 5. 對(duì)于目前正在臨床試驗(yàn)中的 tau 蛋白抗體藥物[5],。
Gosuranemab (戈奈單抗) 是一種人源化 IgG4 單克隆抗 tau 抗體,,靶向細(xì)胞外 tau N 端片段 (eTau),這些片段最初是從家族性 AD 患者來(lái)源的多能干細(xì)胞中分離的,。eTau 被認(rèn)為參與 tau 蛋白病病理學(xué)的傳播,,Gosuranemab 在額顳葉癡呆小鼠模型中中和 eTau 的毒性。結(jié)合實(shí)驗(yàn)表明,,Gosuranemab 對(duì)來(lái)自不同 tau 蛋白病的 tau 單體,、tau 原纖維和不溶性 tau 表現(xiàn)出高親和力。使用 X 射線晶體學(xué)和誘變進(jìn)行的表位定位研究表明,,Gosuranemab 與人 tau15-22 殘基結(jié)合,。
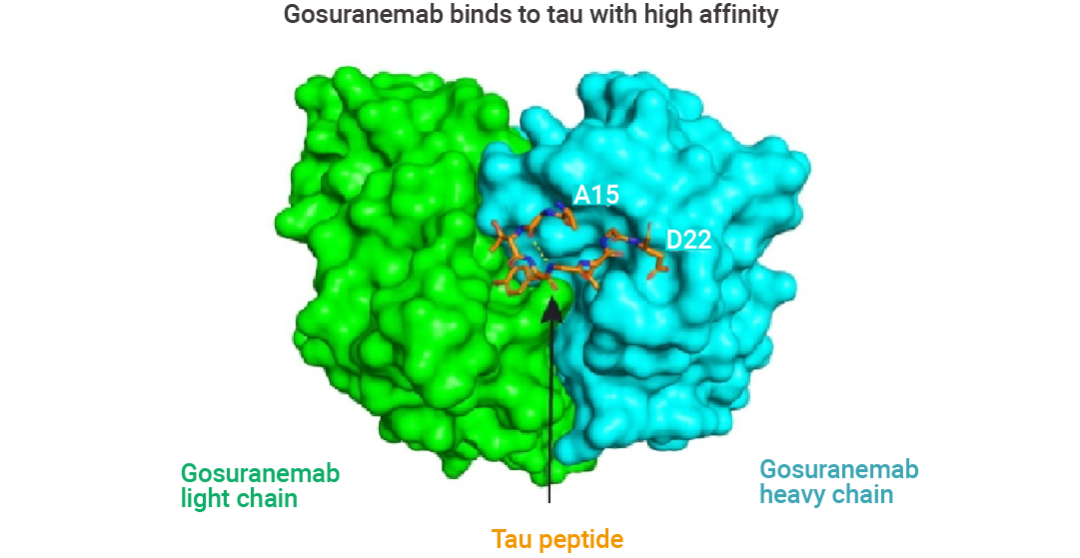
圖 6. Gosuranemab 與 tau 的晶體結(jié)構(gòu)[6]。
青色表示重鏈,,綠色表示輕鏈,,橙色表示 tau 肽,。
Semorinemab (西瑞奈單抗) 是一種 IgG4 單克隆抗 tau 抗體,結(jié)合人 tau 的所有六種亞型的 N 端,,包括單體和寡聚體,,在神經(jīng)元和小膠質(zhì)細(xì)胞共培養(yǎng)中能夠保護(hù)神經(jīng)元免受 tau 寡聚體神經(jīng)毒性的影響。此外在轉(zhuǎn)基因小鼠 tau 病變模型中,,小鼠版本的 Semorinemab 每周一次腹膜內(nèi)給藥 13 周后,,減少 tau 病理的積累,,與抗體效應(yīng)功能狀態(tài)無(wú)關(guān),。在 1 期臨床試驗(yàn)中,單劑量高達(dá) 16,800 mg,,一個(gè)月內(nèi)多劑量總計(jì) 33,600 mg,,沒(méi)有觀察到令人擔(dān)憂的安全信號(hào)。與健康對(duì)照參與者相比,,AD 參與者在服藥后觀察到系統(tǒng)性 tau 濃度更高,。
Tilavonemab (替拉奈單抗) 是一種人源化 IgG4 抗體,它識(shí)別一種聚集的細(xì)胞外病理性 tau 形式,,與 tau 的 N 端結(jié)合,。Tilavonemab 與其他一些抗 tau 抗體的不同之處在于,其作用機(jī)制不需要被神經(jīng)元攝取,。在 P301S tau 轉(zhuǎn)基因小鼠中,,Tilavonemab 可以減少腦神經(jīng)原纖維病理、不溶性 tau,、小膠質(zhì)細(xì)胞增生,、處理過(guò)的腦裂解物的接種活性和條件性恐懼反應(yīng)的缺陷。在一項(xiàng) 1 期單次遞增劑量研究 (NCT02494024) 和一項(xiàng) 2 期隨機(jī)安慰劑對(duì)照試驗(yàn) (NCT02985879) 中,,Tilavonemab 耐受性良好,,但未對(duì)患者有效。
Zagotenemab (澤格特奈單抗) 是人源化 IgG4 抗體,,靶向源自 MCI-1 的 tau 的 7-9 和 312-342 個(gè)氨基酸,。Zagotenemab 結(jié)合并中和可溶性 tau 聚集體。在臨床前研究中,,通過(guò)涉及轉(zhuǎn)基因小鼠和非人靈長(zhǎng)類動(dòng)物的研究,,突出了 Zagotenemab 親本抗體的療效。當(dāng)轉(zhuǎn)基因小鼠用 MCI-1 處理時(shí),,觀察到磷酸化 tau 水平和神經(jīng)原纖維病理顯著降低,。這種效應(yīng)歸因于 tau/抗體復(fù)合物的清除,由小膠質(zhì)細(xì)胞依賴性或神經(jīng)元依賴性機(jī)制,。此外,,與單體相反,,它表現(xiàn)出與 tau 聚集體的選擇性和高親和力結(jié)合。在非人靈長(zhǎng)類動(dòng)物中,,Zagotenemab 在血清中的半衰期為 13 天,,清除率為 0.15 mL/h/kg。
Bepranemab (貝瑞奈單抗) 是一種人源化單克隆 IgG4 抗體,,與 tau 的中心區(qū)域結(jié)合,,識(shí)別 tau 微管結(jié)合結(jié)構(gòu)域附近的 235-250 氨基酸。與 N 末端靶向的抗 tau 抗體相比,,Bepranemab 更干擾致病性聚集性 tau 的細(xì)胞間傳播與靶向 tau N 端區(qū)域的抗體相比,,靶向 tau 中區(qū)的抗體似乎更有可能破壞病原性和聚集的 tau 在細(xì)胞之間的傳遞。在轉(zhuǎn)基因小鼠的實(shí)驗(yàn)中,,它成功地避免了通過(guò)注射源自阿爾茨海默病腦提取物的 tau 誘導(dǎo)的 tau 病理學(xué)的發(fā)作,。此外,它還證明了阻止 tau 病理學(xué)傳播到遠(yuǎn)處大腦區(qū)域的能力,。另一個(gè)重要方面是其人 IgG4 種型,,表明消除與抗體結(jié)合的 tau 可能不依賴于小膠質(zhì)細(xì)胞吞噬作用。這種特征為其在減輕與 tau 蛋白相關(guān)的神經(jīng)退行性病變引入了額外的復(fù)雜性,。
Posdinemab (JNJ-63733657) 是一種人源化 IgG1 單克隆抗體,,結(jié)合富含脯氨酸的 tau 結(jié)構(gòu)域。與靶向 tau 的 N 端的抗體相比,,Posdinemab 更能有效地干擾致病性聚集的 tau 的細(xì)胞間傳播,。它對(duì)在殘基 217 處磷酸化的 tau 具有高親和力。Posdinemab 可在基于細(xì)胞的測(cè)定中消除致病性 tau“種子”,,并抑制小鼠模型中 tau 病理學(xué)的擴(kuò)散,。
MCE 為廣大客戶提供高質(zhì)量,高純度的抗體抑制劑產(chǎn)品,,包括:?jiǎn)慰寺】贵w,、雙特異性抗體、融合蛋白,、大鼠/小鼠體內(nèi)抗體,、同型對(duì)照抗體等,經(jīng) SDS-PAGE,,SEC-HPLC 驗(yàn)證純度大于 95%,,內(nèi)毒素小于 1 EU/mg,可用于體內(nèi)研究,。
產(chǎn)品推薦 |
β-Amyloid (25-35) HY-P0128 β-Amyloid (25-35) (Amyloid beta-peptide (25-35)) 是阿爾茨海默氏淀粉樣蛋白 β 肽的 Aβ (25-35) 片段,,在培養(yǎng)細(xì)胞中顯示出神經(jīng)毒性活性。 |
β-Amyloid (1-42), human HY-P1363A β-Amyloid (1-42), human (Amyloid β-peptide (1-42), human) 是由 42 個(gè)氨基酸組成的肽,,其在阿爾茨海默病的發(fā)病機(jī)制中起關(guān)鍵作用,。 |
Lecanemab (Mouse IGG2a) HY-P990110 Lecanemab (Mouse IGG2a) 是一種靶向可溶性 β-amyloid 的單克隆抗體,,具有減輕認(rèn)知下降的作用。 |
Semorinemab HY-P99399 Semorinemab (RG 6100) 是一種抗 Tau 人源化 IgG4 單克隆抗體,,靶向 Tau 蛋白的 N 端部分 (氨基酸殘基 6-23),。 |
Gantenerumab HY-P99022 Gantenerumab 是一種人源的抗淀粉樣蛋白-β (Aβ) IgG1 單克隆抗體,顯示出持續(xù)的腦淀粉樣蛋白-β 結(jié)合,。 |
Aducanumab HY-P9967 Aducanumab (BIIB037) 是一種選擇性靶向聚集的 β 淀粉樣蛋白 (Aβ) 的人單克隆抗體,。 |
Bapineuzumab HY-P99185 Bapineuzumab 是一種抗 β-淀粉樣蛋白 (APP) 單克隆抗體。Bapineuzumab 可用于阿爾茨海默病 (AD) 的研究,。 |
Bepranemab HY-P99471 Bepranemab (UCB 0107) 是一種人源化全長(zhǎng) IgG4 單克隆抗體,。Bepranemab 靶向 tau 蛋白的中心部分,特別是 235 至 246 位氨基酸,。Bepranemab 可用于阿爾茨海默病 (AD) 研究,。 |

[1] Qi X, et al. Disease Modifying Monoclonal Antibodies and Symptomatic Pharmacological Treatment for Alzheimer's Disease. Biomedicines. 2024 Nov 19;12(11):2636.
[2] Esang M, et al. Aducanumab as a Novel Treatment for Alzheimer's Disease: A Decade of Hope, Controversies, and the Future. Cureus. 2021 Aug 31;13(8):e17591.
[3] Chowdhury S, et al. Novel anti-amyloid-beta (Aβ) monoclonal antibody lecanemab for Alzheimer's disease: A systematic review. Int J Immunopathol Pharmacol. 2023 Jan-Dec;37:3946320231209839.
[4] Sperling RA, et al. Trial of Solanezumab in Preclinical Alzheimer's Disease. N Engl J Med. 2023 Sep 21;389(12):1096-1107.
[5] Imbimbo BP, et al. Initial failures of anti-tau antibodies in Alzheimer's disease are reminiscent of the amyloid-β story. Neural Regen Res. 2023 Jan;18(1):117-118.
[6] Sopko R, et al. Characterization of tau binding by gosuranemab. Neurobiol Dis. 2020 Dec;146:105120.

相關(guān)產(chǎn)品
免責(zé)聲明
- 凡本網(wǎng)注明“來(lái)源:化工儀器網(wǎng)”的所有作品,均為浙江興旺寶明通網(wǎng)絡(luò)有限公司-化工儀器網(wǎng)合法擁有版權(quán)或有權(quán)使用的作品,,未經(jīng)本網(wǎng)授權(quán)不得轉(zhuǎn)載、摘編或利用其它方式使用上述作品,。已經(jīng)本網(wǎng)授權(quán)使用作品的,,應(yīng)在授權(quán)范圍內(nèi)使用,并注明“來(lái)源:化工儀器網(wǎng)”,。違反上述聲明者,,本網(wǎng)將追究其相關(guān)法律責(zé)任。
- 本網(wǎng)轉(zhuǎn)載并注明自其他來(lái)源(非化工儀器網(wǎng))的作品,,目的在于傳遞更多信息,,并不代表本網(wǎng)贊同其觀點(diǎn)和對(duì)其真實(shí)性負(fù)責(zé),不承擔(dān)此類作品侵權(quán)行為的直接責(zé)任及連帶責(zé)任,。其他媒體,、網(wǎng)站或個(gè)人從本網(wǎng)轉(zhuǎn)載時(shí),必須保留本網(wǎng)注明的作品第一來(lái)源,,并自負(fù)版權(quán)等法律責(zé)任,。
- 如涉及作品內(nèi)容、版權(quán)等問(wèn)題,,請(qǐng)?jiān)谧髌钒l(fā)表之日起一周內(nèi)與本網(wǎng)聯(lián)系,,否則視為放棄相關(guān)權(quán)利。
 手機(jī)版
手機(jī)版 化工儀器網(wǎng)手機(jī)版
化工儀器網(wǎng)手機(jī)版
 化工儀器網(wǎng)小程序
化工儀器網(wǎng)小程序
 官方微信
官方微信 公眾號(hào):chem17
公眾號(hào):chem17
 掃碼關(guān)注視頻號(hào)
掃碼關(guān)注視頻號(hào)

















 采購(gòu)中心
采購(gòu)中心