聯(lián)系電話
- 聯(lián)系人:
- 曹女士
- 電話:
- 400-6111-883
- 手機:
- 售后:
- 4006-111-883
- 傳真:
- 86-21-34615995
- 地址:
- 上海市浦東新區(qū)天雄路166弄1號3樓
- 網(wǎng)址:
- www.yeasen.com
掃一掃訪問手機商鋪
內(nèi)毒素的概念
已知,,凡是能造成生物機體體溫上升的物質(zhì)均可稱為熱原(Pyrogen),,其來源可能多樣化。而細菌內(nèi)毒素(Endotoxin)是熱原的一種,,它是細菌性感染的一個重要致病因素,。
內(nèi)毒素是革蘭氏陰性菌菌體中存在的毒性物質(zhì)總稱,為多種革蘭氏陰性菌細胞壁上的teyou結(jié)構(gòu),。細菌內(nèi)毒素主要由磷脂,、脂蛋白和脂多糖(LPS)組成,其中脂多糖(LPS)是天然或?qū)嶒炇抑苽涞膬?nèi)毒素復(fù)合物的生物活性部分,,發(fā)揮毒性作用的是類脂質(zhì)A(Lipid A),。不同革蘭氏陰性菌的脂質(zhì)A結(jié)構(gòu)基本相似,所以由此類細菌引起的感染導(dǎo)致的毒性效應(yīng)大致相同,,主要表現(xiàn)為發(fā)熱,、微循環(huán)障礙、內(nèi)毒素休克及播散性血管內(nèi)凝血等,。細菌在存活狀態(tài)時不會釋放內(nèi)毒素,,但當細菌死亡裂解或者自溶后,內(nèi)毒素會被大量釋放出來,。

圖1.革蘭氏陰性菌結(jié)構(gòu)圖
細菌內(nèi)毒素耐熱性和化學(xué)穩(wěn)定性很強,,一般的方法很難將其去除或滅活,如:常規(guī)高壓滅菌法也不能將內(nèi)毒素chedi清除,,一般的化學(xué)藥品也不會影響細菌內(nèi)毒素的活性,,只有強酸、強堿或強氧化劑可以破壞其結(jié)構(gòu),。但內(nèi)毒素具有水溶性,,生產(chǎn)中可用無熱原水沖洗以除去熱原;其還具有被吸附性,,可用活性碳將其吸附,。
細菌內(nèi)毒素是目前最危險和最常見的致熱污染物之一,,主要原因為:它在自然界中無處不在(革蘭氏陰性菌即使在干凈的水中也能繁殖)、毒性強,、在jiduan條件下也很穩(wěn)定,、生產(chǎn)過程中很容易引入。對于日常的生命科學(xué)實驗,,使用細菌制備的質(zhì)粒DNA和重組蛋白中都會有內(nèi)毒素的殘留,,而且很難去除干凈,進而對后續(xù)實驗帶來潛在毒性影響,。內(nèi)毒素的主要成分脂多糖有強烈的免疫活性和細胞毒性并產(chǎn)生復(fù)雜的細胞生物學(xué)效應(yīng),,因此大多數(shù)情況下會明顯干擾并產(chǎn)生不可預(yù)測的實驗結(jié)果。對生物系統(tǒng),,當人(或動物)體血液系統(tǒng)的輸入液中混入微量的細菌內(nèi)毒素時,,可激活組織內(nèi)的炎性細胞和炎癥因子,導(dǎo)致機體發(fā)熱并產(chǎn)生全身性炎癥反應(yīng),,在很短時間內(nèi)將會使人產(chǎn)生昏迷和高燒,,若不及時搶救,很可能危及生命,。
因此,,無論是用于生命科學(xué)研究的可能含有內(nèi)毒素的相關(guān)試劑,還是用于人和動物預(yù)防或治療的化學(xué)藥品,、抗生素,、生物制品等的原輔料、中間品和放行產(chǎn)品均需要進行內(nèi)毒素檢測,,以確保有效性和安全性,。
內(nèi)毒素檢測及法規(guī)監(jiān)管要求
從20世紀開始,內(nèi)毒素檢測方法相繼出現(xiàn),。
1942年,,美國藥典首先收載家兔法檢測熱原(RPT法)。該方法可以檢測所有類型的熱原物質(zhì),;但有其缺點,,即動物個體差異大導(dǎo)致檢測靈敏度低,對于毒性大的藥物如放射性藥物或腫瘤抑制劑等無法進行檢測,,是定性而非定量方法,,不能用于藥品生產(chǎn)過程中的質(zhì)量控制。
1980年,,F(xiàn)DA發(fā)布用鱟試劑來檢測人用和獸用注射藥成品的內(nèi)毒素,;同年,《美國藥典》收載細菌內(nèi)毒素檢測法,,但在藥典各品種正文中未涉及,。
1995年,,美國藥典23版1至7增補本除了經(jīng)典的凝膠法(LAL)外,還收載了動態(tài)濁度法,、動態(tài)顯色法,、終點顯色法。
2005年版《中國藥典》也有規(guī)定熱原檢查采用家兔法,,細菌內(nèi)毒素檢查采用鱟試劑法,。鱟試劑法具有易操作、靈敏度高,、可用于內(nèi)毒素定量檢測等優(yōu)點,但也有其不便之處,,如:鱟血批次間有差異,,對革蘭氏陰性菌以外的內(nèi)毒素不靈敏,易受β-葡聚糖(β-Glucans)影響而產(chǎn)生假陽性,,鱟受到動物保護,,無法大批量供應(yīng)。
鑒于上述情況,,國內(nèi)外藥典法規(guī)也提出了一些新的內(nèi)毒素檢測方法,。如:2020版《中國藥典》(四部)9251章節(jié)中提到可以采用重組C因子法檢測細菌內(nèi)毒素(C因子是鱟試劑中對細菌內(nèi)毒素敏感的蛋白,能夠選擇性識別內(nèi)毒素),。美國藥典(USP)專家委員會也已于2024年7月26日批準將USP<86>Bacterial Endotoxins Test Using Recombinant Reagents納入《美國藥典-國家處方集》,,USP<86>章節(jié)于2024年11月發(fā)布,并于2025年5月正式生效,。重組C因子法(rFc)通過重組方法產(chǎn)生C因子,,具有:C因子來源穩(wěn)定,受批次影響??;操作簡單快速;更強的抗干擾能力(不受β-glucans影響),;專屬性好等優(yōu)點,。該方法也有其缺點,主要為來源于不同品質(zhì)鱟血蛋白序列的重組蛋白對內(nèi)毒素的反應(yīng)性可能不同,。
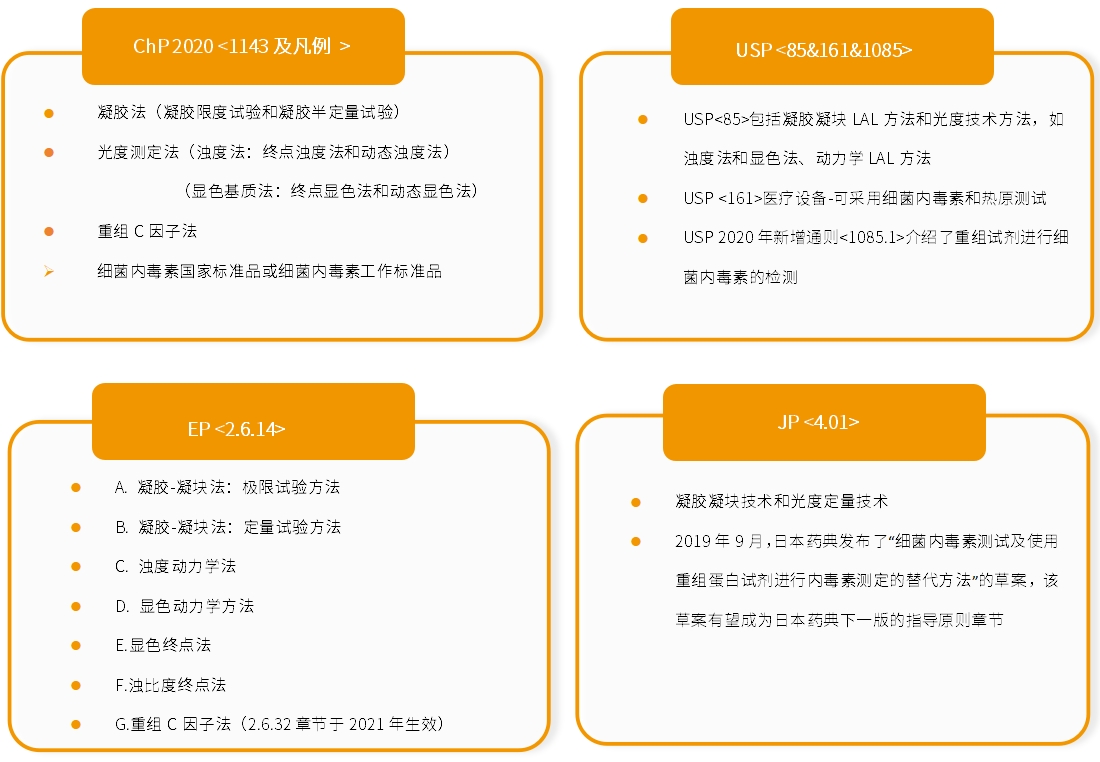
圖2.中外法規(guī)里列舉的內(nèi)毒素檢測方法
重組C因子內(nèi)毒素檢測方法
2020版《中國藥典》(三部)針對細菌內(nèi)毒素檢測,,收錄了包括凝膠法和光度法在內(nèi)的共6種細菌內(nèi)毒素檢查方法。
凝膠法和光度法等都需要從海洋節(jié)肢動物鱟中取鱟血作為原料,,而鱟目前已呈瀕?,F(xiàn)狀,亟需尋求替代方法,。2020版《中國藥典》(四部)9251章節(jié)中提到可以采用重組C因子法檢測細菌內(nèi)毒素,。此外,,美國、歐洲和日本藥典也都提到可以采用重組C因子法檢測細菌內(nèi)毒素,。
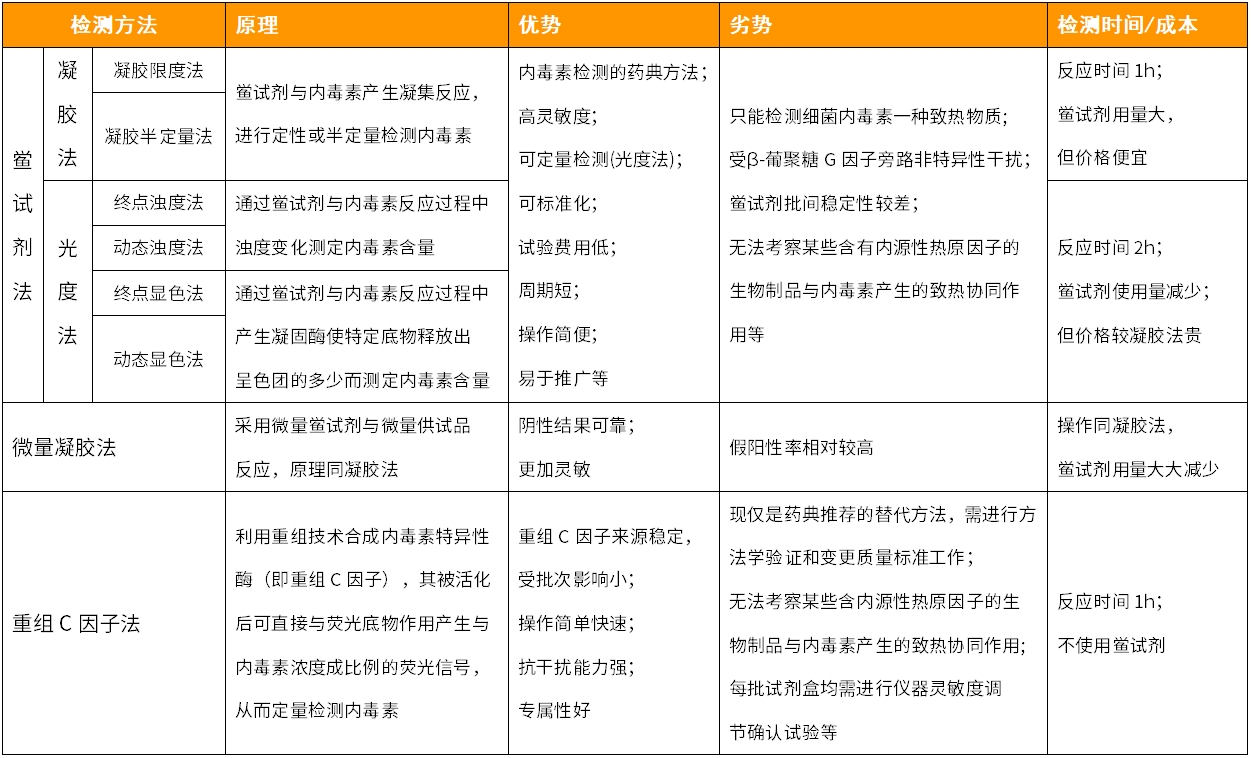
表1.各種內(nèi)毒素檢測方法介紹
目前,,行業(yè)內(nèi)對于內(nèi)毒素的檢測,雖然仍以鱟試劑方法為主,,但也逐漸接受重組C因子的檢測方法,。為此,翌圣生物自主研發(fā)了重組C因子內(nèi)毒素檢測試劑盒,。
本試劑盒通過基因重組的方式表達C因子,,然后重組C因子被待測樣本中的細菌內(nèi)毒素激活,進而酶切水解熒光底物,,產(chǎn)生與內(nèi)毒素濃度成比例的熒光信號,,根據(jù)熒光信號值檢測內(nèi)毒素含量。本試劑盒可以用于人類疾病治療的注射藥物(如化學(xué)藥品,、抗生素,、生物制品等)和醫(yī)療器械(包括透析液、植入式器械等)的原輔料,、研發(fā)和生產(chǎn)工藝過程以及商業(yè)化進程中的內(nèi)毒素檢測,。
產(chǎn)品特點
安全穩(wěn)定:合成試劑,不依賴動物源性成分,,具有更高的批間一致性,、安全性及可持續(xù)性;
強特異性:重組技術(shù)消除了鱟試劑中β-1,3-葡聚糖對檢測結(jié)果的干擾,,提高特異性和準確性,;
高靈敏度:檢測范圍0.005-5EU/mL,定量下限(LLOQ)低至0.005EU/mL,;
高精密度:批內(nèi)重復(fù)性高CV<10%,,批間差異小即中間精密度CV<15%;
快速便捷:僅需1h即可完成檢測,;
驗證完善:參考ICH Q2(R2)分析方法驗證指導(dǎo)原則,,可提供完善的驗證報告。
實驗數(shù)據(jù)
試劑盒檢測范圍為0.005~5EU/mL,,R2=0.9968,,各濃度檢測值CV≤10%。
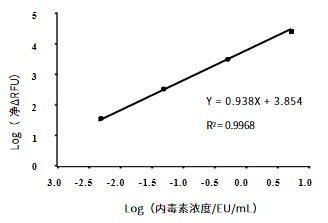
圖3.重組C因子內(nèi)毒素檢測試劑盒標準曲線
該重組C因子內(nèi)毒素檢測試劑盒不受鱟試劑中β葡聚糖的干擾,,避免了因β-葡聚糖引起的假陽性/結(jié)果不準確情況,。
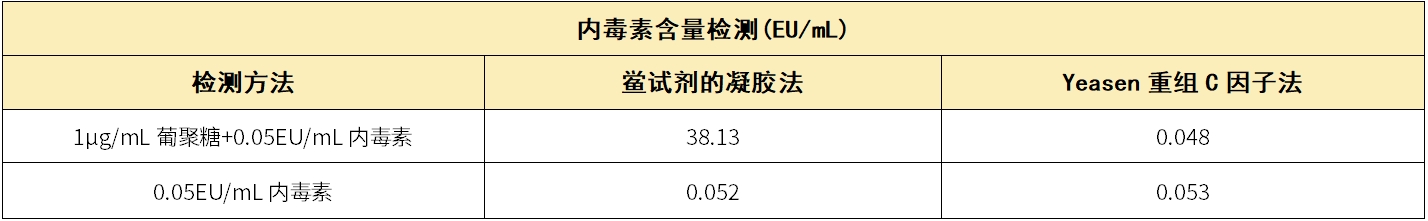
表2.不同內(nèi)毒素檢測方法數(shù)據(jù)對比
產(chǎn)品信息
類別 | 產(chǎn)品 | 貨號 | 品名 | 規(guī)格 |
重組C因子法 內(nèi)毒素檢測 | 重組C因子試劑盒 | 36723ES | Recombinant Factor C Endotoxin Detection Kit 重組C因子內(nèi)毒素檢測試劑盒 | 48 T/96 T |
動態(tài)濁度法 內(nèi)毒素檢測 | 動態(tài)濁度法 內(nèi)毒素試劑 | 60401ES | Kinetic Turbidimetric LAL Assays 動態(tài)濁度法內(nèi)毒素檢測鱟試劑 | 17 T |
內(nèi)毒素去除 | 內(nèi)毒素去除試劑盒 | 60404ES | Endotoxin Removal Kit 內(nèi)毒素去除試劑盒 | 1 Kit |

 初級會員·13年
初級會員·13年
