在制作原代細(xì)胞免疫熒光時(shí),,容易出現(xiàn)一些問(wèn)題,,造成熒光鑒定失敗,將抗原或抗體標(biāo)記上熒光素,,制成熒光抗體檢測(cè)組織或細(xì)胞內(nèi)的相應(yīng)抗原(或抗體)時(shí),,一定要注意抗體的比例高低和濃度。
制作免疫熒光常用的方法有:
方法一:直接法
步驟:將熒光標(biāo)記的特異性抗體(抗原)直接加在抗原(抗體)上,,經(jīng)一定的溫度和時(shí)間染色,,水洗—干燥—封片—鏡檢
優(yōu)點(diǎn):操作簡(jiǎn)便、特異性高,、非特異性染色少
缺點(diǎn):敏感性低
方法二:間接法
步驟:先用已知未標(biāo)記的特異性抗體(一抗)與抗原反應(yīng),,再用標(biāo)記的抗體(二抗)與其反應(yīng),形成抗原—抗體—抗體復(fù)合物,,水洗—干燥—封片—鏡檢
優(yōu)點(diǎn):敏感性強(qiáng),,目前多采用間接法
缺點(diǎn):操作復(fù)雜
實(shí)驗(yàn)過(guò)程中常見(jiàn)的問(wèn)題:
1,整個(gè)細(xì)胞片都出現(xiàn)熒光高點(diǎn)
原因有二:一是二抗?jié)舛冗^(guò)高,,適當(dāng)降低二抗?jié)舛燃纯?。二是二抗發(fā)生沉淀,可以使用過(guò)濾或者離心熒光標(biāo)記二抗
2,,信號(hào)弱或無(wú)信號(hào),,染色細(xì)胞過(guò)少
目標(biāo)蛋白在細(xì)胞中沒(méi)有表達(dá),需要制備細(xì)胞裂解液,,用Western Blotting驗(yàn)證目標(biāo)蛋白在細(xì)胞中是否表達(dá),。
表達(dá)目標(biāo)蛋白的細(xì)胞過(guò)少,標(biāo)本中使用更多的細(xì)胞,,試用其他瞬時(shí)轉(zhuǎn)染方法,,或者使用穩(wěn)定轉(zhuǎn)染細(xì)胞系。
細(xì)胞通透性差,,需要增加通透劑作用的時(shí)間或者濃度,,或改用其它的通透劑
染色前的固定步驟破壞了抗原表位,,改用其他固定方法,。
通透使抗原丟失,可以減少通透劑作用的時(shí)間或強(qiáng)度,。
抗體不識(shí)別,,需要換用其他抗體
一抗稀釋度過(guò)大,使用同一樣品按*的二抗用量作一抗稀釋曲線,,以確定*的一抗稀釋比例,。
二抗選擇錯(cuò)誤,要使用正確的二抗
3,鏡下觀察只有DAPI的藍(lán)光,,目的熒光幾乎沒(méi)有或者很弱
出現(xiàn)這種現(xiàn)象很有可能是抗體比例太低,,需提高抗體濃度,可配合提高二抗?jié)舛?;共聚焦的激發(fā)熒光強(qiáng)度不夠大,;二抗孵育時(shí)是否是對(duì)應(yīng)的種屬,比如本來(lái)需要山羊抗鼠結(jié)果加為山羊抗兔,。
4,,細(xì)胞核周圍總是存在有一些藍(lán)色的小點(diǎn)點(diǎn)
這種情況一般是支原體污染所致,建議用殺支原體藥2周后再檢測(cè),,或者通過(guò)提高共聚焦機(jī)器背景值來(lái)覆蓋支原體熒光
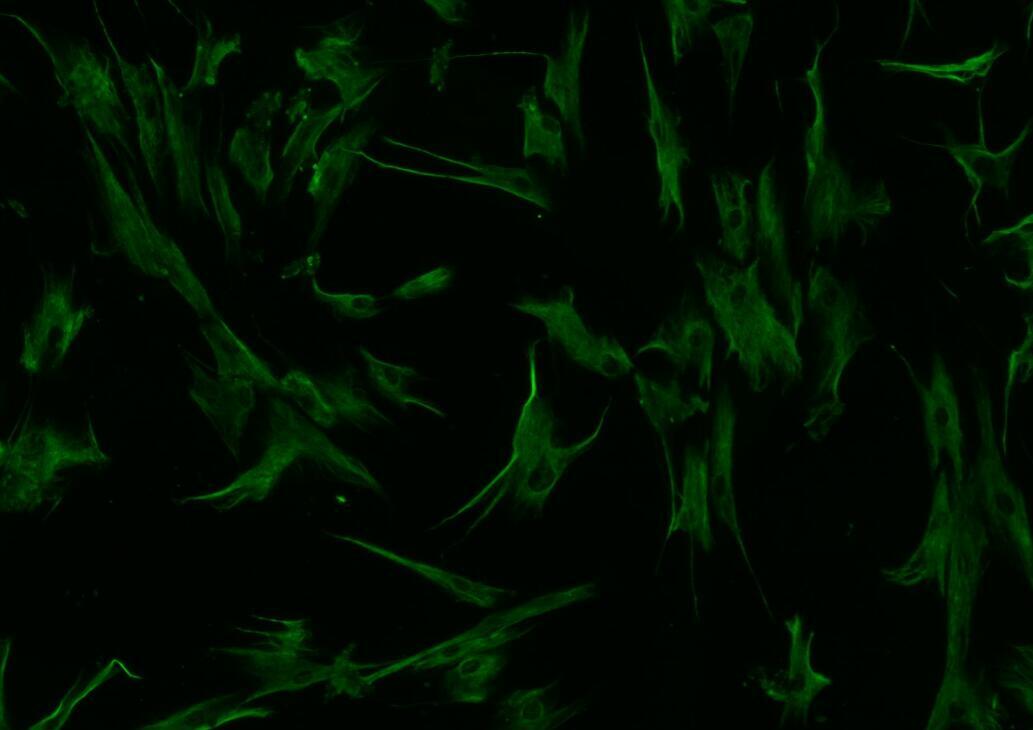
5,,如何共定位的視野
共定位時(shí),首先判斷哪些細(xì)胞是轉(zhuǎn)染成功的,,比如我過(guò)表達(dá)了蛋白A,,想做蛋白A和蛋白B的共定位關(guān)系,則在視野中尋找已成功轉(zhuǎn)染蛋白A的細(xì)胞,,一般熒光強(qiáng)度會(huì)顯著高于周邊其他細(xì)胞,,再在這個(gè)細(xì)胞上觀察蛋白B的表達(dá)。
6,,視野中細(xì)胞與細(xì)胞之間存在散在的發(fā)光點(diǎn)
有兩種情況可造成:1,,拍照時(shí)PBS量過(guò)少引起的非特異性;2,,PBS未過(guò)濾,,未溶解的殘?jiān)じ蕉鴮?dǎo)致
三、除此之外,,這些注意事項(xiàng)也要牢記
1,、合適的抗體稀釋比例
通過(guò)優(yōu)化抗體稀釋比例來(lái)優(yōu)化染色,通常情況下1ug/ml的純化抗體或者1:100-1:1000的抗血清足夠達(dá)到特異性染色的結(jié)果,。但在能保證低背景染色的前提下,,可以通過(guò)增加濃度來(lái)提高信號(hào)強(qiáng)度。如果是*次使用該抗體或測(cè)定某抗原,,強(qiáng)烈建議濃度梯度實(shí)驗(yàn),。
2、抗體特異性
免疫熒光需要用到特異性非常強(qiáng)的抗體,,可以避免高背景和不理想的蛋白定位結(jié)果,。在大多數(shù)情況下,純化抗體的效果很好,,但是正確的對(duì)照可以幫助定位抗原,。使用只有二抗染色的片子
3,、細(xì)胞固定和通透
為達(dá)到*的檢測(cè)效果,細(xì)胞需要經(jīng)過(guò)固定和通透,。這些步驟非常關(guān)鍵,,細(xì)胞和抗原需要保證*的結(jié)構(gòu),并利于抗體與抗原結(jié)合,。通常情況下,,需要通過(guò)以下步驟得以實(shí)現(xiàn):細(xì)胞用2%-4%多聚甲醛固定,之后用0.1%皂角苷或0.02%的Triton X-100進(jìn)行通透,。前者是比較溫柔的處理,,但是對(duì)于核內(nèi)抗原可能無(wú)效,需要用到Triton,。使用皂角苷進(jìn)行通透時(shí),,要注意它會(huì)引起細(xì)胞膜的可逆性通透,也就是除了在通透初期,,在每個(gè)抗體孵育環(huán)節(jié)都需要進(jìn)行通透,。另外,細(xì)胞可以用冰甲醇進(jìn)行同時(shí)固定和通透,,可以避免去垢劑的使用,。
4、封閉條件的優(yōu)化選擇
為了防止內(nèi)源性非特異性蛋白抗原的結(jié)合,,需要在一抗孵育前用封閉液封閉,,這樣可以減少非特異性的背景著色。封閉液可以選擇二抗來(lái)源一致的血清,,一般來(lái)說(shuō),,血清價(jià)格比較昂貴,可以用1%-5%BSA替代,,BSA可以說(shuō)是的封閉血清,。另外封閉時(shí)間不易過(guò)長(zhǎng),30-60min即可,,且封閉后不用洗滌,,直接加一抗孵育即可。
5,、一抗二抗的選擇
封閉過(guò)后需要一抗孵育,,可以選擇4度過(guò)夜孵育或者室溫3h,以筆者的經(jīng)驗(yàn)是一抗孵育4度過(guò)夜比較好,,抗原抗體結(jié)合會(huì)比較充分,。一抗二抗的稀釋比例可以根據(jù)抗體說(shuō)明書(shū)來(lái),,再根據(jù)自己具體的實(shí)驗(yàn)要求進(jìn)行優(yōu)化,。如果抗體濃度過(guò)低,會(huì)造成信號(hào)太弱,如果抗體濃度過(guò)高可能會(huì)造成背景染色太強(qiáng),。熒光二抗個(gè)人感覺(jué)Alex flour熒光基團(tuán)信號(hào)強(qiáng)于Dylight強(qiáng)于FITC,。如果做免疫雙標(biāo),一抗要來(lái)自不同種屬,,熒光二抗的光譜也要分開(kāi),。
(空格分隔,最多3個(gè),單個(gè)標(biāo)簽最多10個(gè)字符)
立即詢價(jià)
您提交后,專屬客服將第一時(shí)間為您服務(wù)